Logran que los glóbulos blancos alivien el dolor, en lugar de producirlo, durante la inflamación de los tejidos en ratones
Fuente: Universidad de Granada

Los miembros del grupo de investigación de la UGR que han realizado este trabajo. De izquierda a derecha, Miguel Ángel Tejada Giráldez, Ángeles Montilla García, M Carmen Ruiz Cantero y Enrique J. Cobos del Moral.
Las células del sistema inmune, los leucocitos o glóbulos blancos, se acumulan en los tejidos del cuerpo humano tras, por ejemplo, sufrir un traumatismo o una herida. Su función principal es la reparación de este tejido dañado. Sin embargo, además de esta función de reparación, estas células producen ciertas sustancias que promueven el dolor (denominadas algógenos), por lo que juegan un papel clave en el dolor que se siente cuando el tejido está inflamado. Esto es también aplicable a ciertas patologías crónicas que cursan con inflamación y dolor, como en el caso de las artritis.
Paradójicamente, estos leucocitos además de liberar algógenos, son capaces de producir péptidos opioides endógenos (como las endorfinas). Estos péptidos tienen la misma actividad que los analgésicos opioides (fármacos para tratar el dolor intenso, como la morfina), que se usan desde hace milenios para tratar el dolor. Sin embargo, el balance entre la actividad de los leucocitos a favor y en contra del dolor durante la inflamación favorece claramente al dolor; de hecho, la inflamación produce dolor.
El receptor sigma-1 es una proteína muy pequeña presente en las neuronas, y es capaz de modular la acción de los receptores opioides. En un estudio liderado por científicos de la Universidad de Granada (pertenecientes al departamento de Farmacología e Instituto de Neurociencias del Centro de Investigación Biomédica, Instituto Biosanitario de Granada), junto con la empresa farmacéutica Esteve, el Instituto Teófilo Hernando de I+D del Medicamento, y el Instituto de Biotecnología Molecular de Austria, se ha descubierto que los bloqueantes del receptor sigma-1 son capaces de incrementar el efecto de estos péptidos opioides endógenos que producen los leucocitos, de manera que estas células del sistema inmune cuando están en el tejido inflamado alivien el dolor en lugar de producirlo.
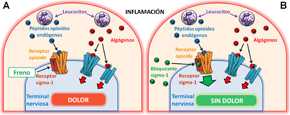
Papel del receptor sigma-1 en el dolor inflamatorio. (A) Los leucocitos presentes en la zona inflamada liberan algógenos que contribuyen al dolor, junto con péptidos opioides endógenos. Estos péptidos opioides no alivian el dolor porque el receptor sigma-1 frena el funcionamiento de los receptores opioides. (B) Los bloqueantes sigma-1 quitan el freno al funcionamiento de los receptores opioides, resultando en el alivio del dolor.
“Estamos ante un mecanismo de alivio del dolor totalmente novedoso, basado en maximizar el potencial analgésico de las células del sistema inmune, y que podría tener importantes aplicaciones terapéuticas en pacientes con dolor de origen inflamatorio”, afirma el director de este trabajo, el investigador del departamento de Farmacología e Instituto de Neurociencias de la Universidad de Granada Enrique J. Cobos del Moral.
Este trabajo de investigación ha sido posible gracias al Programa de Reincorporación de Doctores del Vicerrectorado de Investigación y Transferencia de la UGR.
Referencia bibliográfica:
Sigma-1 receptors control immune-driven peripheral opioid analgesia during inflammation in mice
Miguel A. Tejada, Angeles Montilla-García, Shane J. Cronin, Domagoj Cikes, Cristina Sánchez-Fernández, Rafael González-Cano, M. Carmen Ruiz-Cantero, Josef M. Penninger, José M. Vela, José M. Baeyens and Enrique J. Cobos
Proceedings of the National Academy of Sciences of the United States of America (PNAS), 2017. doi: 10.1073/pnas.1620068114
Contacto:
Enrique J. Cobos del Moral
Departamento de Farmacología e Instituto de Neurociencias de la Universidad de Granada
Tel: 958 24 93 02
Móvil: 610 763 392
Correo electrónico: ejcobos@ugr.es
Últimas publicaciones
Gómez Villamandos fue presidente de la Fundación Descubre desde diciembre de 2022. Durante su etapa al frente de la Consejería impulsó una profunda transformación del sistema universitario y científico andaluz, dejando sentadas las bases del futuro. Entre sus principales hitos destacan la aprobación de la nueva Ley Universitaria para Andalucía.
Sigue leyendoUn estudio de la Universidad de Córdoba revela las motivaciones del sector agrícola andaluz para adoptar prácticas ecológicas en una tierra que concentra el 50% de este tipo de cultivos a nivel nacional.
Una docena de talleres y observaciones se llevarán a cabo en localidades de las provincias de Cádiz, Sevilla, Huelva, Málaga, Jaén y Granada. El plazo de inscripción en esta iniciativa continúa abierto.
Sigue leyendo



